�����J���E�x����
- Home
- �����J���E�x����
- �����J��
- Tox-Omics�ɂ������g
�����J��
Tox-Omics�ɂ������g
- �͂��߂�
- Tox-Omics�̌������e
- ��������
�@Tox-Omics�Ŏg�p�����v���g�R�[��
�A �팱�����ꗗ�y�ѓ����������� - ��`�q�����ʉ��
�@�}�C�N���A���C�����i�T�v�j
�A�}�C�N���A���C�f�[�^��́i�T�v�j
�B���\�ς݃}�C�N���A���C�f�[�^ - Tox-Omics�ŊJ����������E�\�����s�����߂̃v���g�R�[��
- �O�����\
���͂��߂�
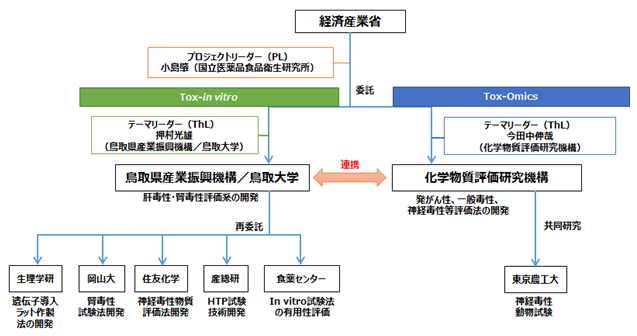
�@2011�N�x�Ɍo�ώY�ƏȂ̎��ƂƂ���5���N�́uARCH-Tox�v�v���W�F�N�g*1���n�܂�܂����B
�@ARCH-Tox�v���W�F�N�g�́A�������i�H�i�q�������� ���S���������������Z���^�[���S���\���]�����̏������������v���W�F�N�g���[�_�[�Ƃ��āAin vivo�ł̈�`�q������͓��̃I�~�N�X�Z�p�Ɋ�Â������@�J�����s���uTox-Omics*2�v�T�u�v���W�F�N�g�ƁAin vitro�̎����@�J�����s���uTox-in vitro*3�v�T�u�v���W�F�N�g�ō\������Ă���A���w�����̗L�Q����]�����邽�߂̐v���������I�Ȏ�@�̊J�������s�����Ƃ�ړI�Ƃ��Ă��܂��B
�@Tox-Omics��2001-2005�N�x�Ɏ��{���ꂽNEDO���Ɓu���@�\�ȈՌ^�L�Q���]����@�̊J���^��`�q������͋Z�p��p���������\����@�̊J���v���x�[�X�ɁA�X�ɐt���ɂ����锭���A�_�o�Ő����̐V���ȃG���h�|�C���g���������T�u�v���W�F�N�g�ł��B�܂��ATox-in vitro��2006-2010�N�x�Ɏ��{���ꂽNEDO�ł�in vitro�����@�J���̃v���W�F�N�g�̌�p�Ƃ��āA�̓Ő��A�t�Ő��A�_�o�Ő�����������ꂽ�T�u�v���W�F�N�g�ł��B
*1 �o�ώY�ƏȂ́u�Ζ������������̐V���ȉ��w�����K���ɕK�v�ȍ��ې擱�I�L�Q�������@�̊J���v�̌ď�
*2 ARCH-Tox�v���W�F�N�g�ɂ�����u�����J�����ڇ@��`�q�����ϓ��f�[�^����e��Ő��̔����\�����擾�����@�̊J���v�̌ď�
*3 ARCH-Tox�v���W�F�N�g�ɂ�����u�W�I����Ő����̓Ő���q�g��Ӌ@�\�̉e�������o������זE�����@(in vitro �����@)�̊J���y�сA����玎���@���̕����̍זE�����@��v���������I�Ɏ��{�\��HTP�����V�X�e���̊J���v�̌ď�
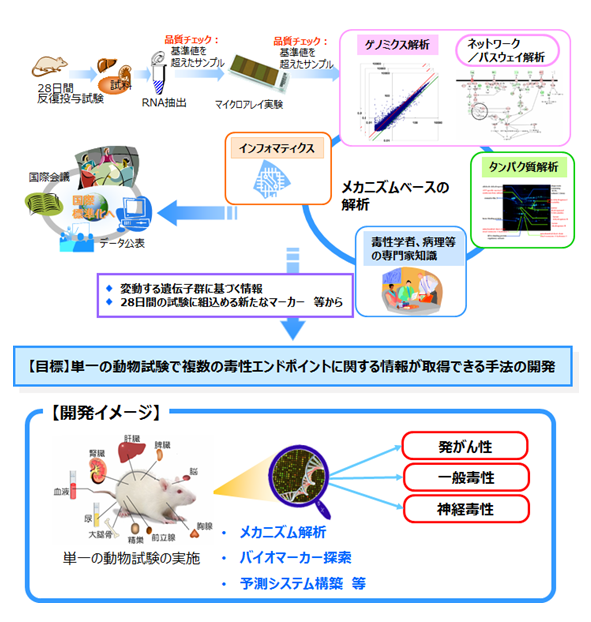
��Tox-Omics�̌������e
�@Tox-Omics�ł́A�P��̓��������œ����鑟��T���v������p���āA���̈�`�q�����ʂ̕ω��𑨂��邱�Ƃɂ��A�����A��ʓŐ��A�_�o�Ő����̑��l�ȓŐ��G���h�|�C���g�Ɋւ�������@���J�����邱�Ƃ�ړI�Ƃ��Ă��܂��B��̓I�ɂ́A28���Ԕ����o�����^�Ő����� (��F���R�@�X�N���[�j���O�Ő������AOECD�e�X�g�K�C�h���C��407) �݂̂ŁA�����̓Ő������o���鎎���n���\�z���邽�߂ɁA���̓��Ő������`�q�����ϓ��Ɗe�Ő��e���Ƃ̊֘A�𑨂��邽�߂̎��݂�i�߂܂����B�����y�ш�ʓŐ��ɂ��ẮA������ɂ����Ă��A�ł��W�I���������̑��y�ѐt���Ɋւ����g���s���܂����B�܂��A�_�o�Ő��ɂ��ẮA�{�v���W�F�N�g�ł̓t�B�[�W�r���e�B�����ƈʒu�Â��A����̔]���ʂɒ��ڂ�����͂��s���ƂƂ��ɁA�]����28���Ԕ������^�Ő������ł͕]��������ł��������B�_�o�Ő��ɂ��Ă��A28���Ԕ������^�Ő������̘g�g�݂Œm���邽�߂̎�g���i�߂܂����B
�@�ŏI�I�ɂ́A�ő�ł�28���Ԃ̓��^�݂̂Ŕ����A�_�o�Ő��ȂǑ���ɂ킽��Ő��e�����A�]�����������x���Z���Ԃ������̓����ŕ]���\�ƂȂ�A3Rs�ɂ��v���ł��鎎���@�ƂȂ���̂Ɗ��҂���܂��B
����������
�@Tox-Omics�Ŏg�p�����v���g�R�[��
�@Tox-Omics�Ŏ��{�������������͎�ɂ͈ȉ��̃v���g�R�[���Ŏ��{���Ă��܂��B
�Ȃ��ATox-Omics�ł͊J�����s����ʼn��L�̓��������n�ɂ�鎎�����s���Ă��܂����A�]�����s���ۂɂ��ڍׂȃv���g�R�[���ɋL�ڂ̂���ȈՂȓ��������ŕ]�����\�ł��B
| �Q�l�K�C�h���C�� | OECD�e�X�g�K�C�h���C��407 �u�V�K���w�������ɌW�鎎���̕��@�ɂ��āv�ɒ�߂�u�M���ނ�p����28���Ԃ̔������^�Ő������v �������̃K�C�h���C���Ƀf�[�^�擾�̂��߂̃T�e���C�g�Q�̐ݒ蓙��lj� |
|
|---|---|---|
| �����n�� | Crl:CD(SD)�Y���b�g�A���^�J�n��5�T�� | |
| ���^���� �y�уT���v�����O |
28���� ���^��A1���ځA7���ځA14���ځA28���ڂŃT���v�����O |
|
| ���^�o�H | �����o�� | |
| �p�ʐݒ� | 7���Ԃ̗\������ (��ʏ�Ԋώ@�A�̏d����A�U���A�튯�d�ʑ���) �����{���A28���Ԕ������^���Ă��m���⎀�S���̏d�ĂȓŐ��e�����������Ȃ��Ɨ\�z�����p�ʂ����p�ʂƂ��A����5����1���p�ʂƂ��Đݒ�B �܂��A�e�팱�����ɂ����Ĕ}�̑ΏƌQ��ݒ�B |
|
| �Q�\�� | 5�C/�Q (�}�C�N���A���C��͂�3�C/�Q�Ŏ��{) |
|
| �����@ | CO2/O2�����K�X�����iCO2:O2������=4:1�j �\�������Ƃ���3�����ɂ��ăC�\�t���������������{ |
|
| �����������荀�� | �E��ʏ�Ԋώ@ | �P�[�W������o���ۂ̔����A��ɂƂ��Ă̏ڍׂȊώ@�A�A���[�i���ł̍s���̊ώ@ |
| �E�@�\���� | ������ (���o�A���o�A�Ɋo�A���E���ˁA��������)�A���́A�����^���� | |
| �E�̏d���� | ||
| �E�ۉa�ʑ��� | ||
| �E�A���� | �A�ʁA�F���A����A�A�Z�����ApH�A�`���A�P�g���́A���A�����A�A���� | |
| �E���t�w�I���� | �Ԍ������A�w���O���r���Z�x�A�w�}�g�N���b�g�l�A���ϐԌ����e�ρA���ϐԌ����w���O���r���ʁA���ϐԌ����w���O���r���Z�x�A�������A�ԏ�Ԍ������䗦�A���������A�������S�����A�D�����A�����p���A�D�_���A�D����A�P���A��^����F���A�v���g�����r�����ԁA�����������g�����{�v���X�`������ | |
| �E���t�����w�I���� | �A�X�p���M���_�A�~�m�g�����X�t�F���[�[�A�A���j���A�~�m�g�����X�t�F���[�[�A�A���J�����t�H�X�t�@�^�[�[�A�R�����G�X�e���[�[�Ag-�O���^�~���g�����X�y�v�`�_�[�[�A���R���X�e���[���A�g���O���Z���h�A�A�f���f�A�N���A�`�j���A���`���A�A���u�~���AA/G��A�����A���r�����r���A���_�`�_�A���@�����A�J���V�E���A�i�g���E���A�J���E���A���f | |
| �E�a���w�I���� | �U���A�튯�d�ʑ���A�a���g�D�w�I���� | |
| ��`�q�����ʉ�͑Ώۑ��� | �̑��A�t�� | |
�A�팱�����ꗗ�y�ѓ�����������
�@Tox-Omics�ŗp�����팱�����̈ꗗ���ȉ��Ɏ����܂��B�܂��A�̓Ő��y�ѐt�Ő��Ɋւ����͂ɗp�������������ɂ��ẮA���w���������N���b�N����Ƃ��̓��������̕������邱�Ƃ��ł��܂��B�܂��A�����̓����������� (31�����A32�����̃f�[�^) �͊��ɓƗ��s���@�l���i�]���Z�p��Ջ@�\ (NITE) �ɂČ��\����Ă���u�L�Q���]���x���V�X�e�������v���b�g�t�H�[��(HESS)�v�y��HESS-DB (2015�N7����) �Ɏ��ڂ���܂����B
| Chemical Name | ���� | CAS RN | ���^�� (mg/kg/day) |
|---|---|---|---|
| 1,2,3-Trichloropropane | TCP | 96-18-4 | 0�A15�A75 |
| 1,2-Dibromoethane | EBD | 106-93-4 | 0�A15�A75 |
| 1-Amino-2,4-dibromoanthraquinone | ADBAQ | 81-49-2 | 0�A200�A1000 |
| 2,2-Bis(bromomethyl)-1,3-propanediol | DBNPG | 3296-90-0 | 0�A200�A1000 |
| 2-Amino-4-nitrophenol | 4-NAP | 99-57-0 | 0�A150�A750 |
| 4,4’-Thiobis(6-tert-butyl-m-cresol) | TBBC | 96-69-5 | 0�A60�A300 |
| 4-Hydroxy-m-phenylenediammonium dichloride | AMIDOL | 137-09-7 | 0�A20�A100 |
| Anthraquinone | AQ | 84-65-1 | 0�A200�A1000 |
| Benzyl acetate | BA | 140-11-4 | 0�A200�A1000 |
| Bromodichloromethane | BDCM | 75-27-4 | 0�A40�A200 |
| Bromodichloromethane/�C�\�t���������� | BDCM_I | 75-27-4 | 0�A40�A200 |
| Carbon tetrachloride | CCl4 | 56-23-5 | 0�A20�A100 |
| Chlorothalonil | CTN | 1897-45-6 | 0�A100�A500 |
| Cisplatin (�o�����^) | CP (gav.) | 15663-27-1 | 0�A0.75�A3.75 |
| Cisplatin (������) | CP (iv.) | 15663-27-1 | 0�A0.15�A0.75 |
| Dipropylene glycol | DPG | 25265-71-8 | 0�A200�A1000 |
| Ethylenediamine dihydrochloride | En�E2HCl | 333-18-6 | 0�A100�A500 |
| 3-(4-Chlorophenyl)-1,1-dimethylurea [Monuron] | CMU | 150-68-5 | 0�A40�A200 |
| N,N'-Dinitrosopentamethylenetetramine | DNPT | 101-25-7 | 0�A40�A200 |
| N-Nitrosodimethylamine | DMN | 62-75-9 | 0�A0.8�A4 |
| Nitrilotriacetic acid trisodium monohydrate | Na3-NTA-H2O | 18662-53-8 | 0�A200�A1000 |
| Ochratoxin A | OTA | 303-47-9 | 0�A0.2�A1 |
| Phenolphthalein | PP | 77-09-8 | 0�A200�A1000 |
| Phenylbutazone | PBZ | 50-33-9 | 0�A40�A200 |
| Potassium bromate�@(1�`14���ԓ��^.28���ԓ��^) | KBrO3 | 7758-01-2 | 0�A20�A100 |
| Bis(p-chlorophenyl)Sulfone | DCDPS | 80-07-9 | 0�A50�A250 |
| Tricresyl Phosphate (isomer mixture) | TOCP | 1330-78-5 | 0�A40�A200 |
| Tris(2-chloroethyl) Phosphate | TCEP | 115-96-8 | 0�A80�A400 |
| o-Anisidine hydrochloride | o-AH | 134-29-2 | 0�A140�A700 |
| o-Anthranilic acid | 2-AA | 118-92-3 | 0�A200�A1000 |
| o-Nitroanisole | o-NA | 91-23-6 | 0�A80�A400 |
| p-Nitroanisole | pNA | 100-17-4 | 0�A100�A500 |
| tert-Butyl alcohol (28���ԓ��^�ł̓C�\�t���������������{) |
TBA | 75-65-0 | 0�A200�A1000 |

����`�q�����ʉ��
Tox-omics�Ŏ��{������`�q�����ʉ�͈͂ȉ��̃v���g�R�[���Ŏ��{���Ă��܂��B
�܂��A�ڍׂȃv���g�R�[��������������_�E�����[�h�ł��܂��B
�@�@�}�C�N���A���C���� (�T�v)
| �̍ޖ@ | (�̑�) �����哮������������Ĉ��y�������A�d�ʂ𑪒��A�O�����t�̒���������喬���Ƃ��̔��Α������ԑΊp���ɉ�����2�`3 mm���̑g�D�Ђ��̎悵�A�d�ʂ�5�{�ʈȏ��RNAlater®�iAmbion, Inc.�j�ɐZ�� (�t��) �E�t���S�� �����哮������������Ĉ��y�������A���E�ʁX�ɏd�ʂ𑪒��A�E���̒���������������܂ނ悤�ɉ��f��4�`5 mm���̑g�D�Ђ��̎悵�ARNAlater®�ɐZ�� �E�t�����ʕ� �����哮������������Ĉ��y�������A���E�ʁX�ɏd�ʂ𑪒��A�E���̒���������������܂ނ悤�ɉ��f��4�`5 mm���̑g�D�Ђ��̎悵�A�g�D�Ђ���햌����菜������A�����œ��A������������A�������сA�����O�ыy�є玿���Ă��ꂼ��RNAlater®�ɐZ�� |
|---|---|
| Total RNA���o | miRNeasy Mini Kit�@(QIAGEN)��p����total RNA�𒊏o |
| Total RNA�i���m�F | BioAnalyzer 2100 (Agilent; ver. B.02.03) ��p���đ���B�}�C�N���A���C�����ɋ����邱�Ƃ��ł����ł���RIN (RNA Integrity Number)�l��7.0�ł��邱�Ƃ��m�F |
| �}�C�N���A���C���� | Agilent��Tox-plus�A���C��p����1�F�@�v���g�R�[�� (Low Input Quick Amp Labeling Kit�Gversion6.5 Dec. 2009)�ɏ]���A�X�L���i�[�Ōu�����x���X�L���j���O��A�摜�f�[�^���擾 |
�A�@�}�C�N���A���C�f�[�^��� (�T�v)
| �摜�f�[�^�̐��l�� | Feature Extraction(Agilent Technologies ver 10.7.1.1) ��p���ĉ摜�f�[�^�𐔒l�����A�}�C�N���A���C�f�[�^ (���f�[�^�GText�`��) ���擾 |
|---|---|
| �A���C�ԃm�[�}���C�Y | GeneSpring GX (Ver. 12.0) ��p���ăO���[�o���m�[�}���C�[�[�V�����@�Ŏ��{ �E�o�b�N�O���E���h��̌��ʐ������A�Ӗ��̂Ȃ����̒l��0.01�ɒu�����܂� �E�A���C���ƂɁA����l��75%�^�C���̒l��1�ɑ����܂� |
| �t���O�J�E���g | �}�C�N���A���C���f�[�^���ɂ���t���O�������Ƃ�3��ނ̃t���O�t��(Detected�ANot Detected�ACompromised) ���v���[�u���ƂɎ��{ |
| ������Z�o | �m�[�}���C�Y��̃V�O�i���l��p���Ĕ}�̑ΏƌQ�ɑ��铊�^�Q�̈�`�q��������Z�o |
�B ���\�ς݃}�C�N���A���C�f�[�^
| ���e | �f�[�^ �� |
GEO Accession ID | �_�� |
|---|---|---|---|
| 9�T��̗Y���b�g��CO2/O2(4:1)���������y�уC�\�t�������������u��̊̑��̈�`�q�����ʃf�[�^ | 6 | GSE71277 | Differences in gene expression profiles in liver caused by different type of anesthesia; cases of CO2-O2 and isoflurane J. Toxicol. Sci., 40(6), 829-836 |
| 5�T��̗Y���b�g��p�����}�̑ΏƋy�щ�������28���Ԕ������^��̊̑��̈�`�q�����ʃf�[�^ | 60 | GSE87147 | Chemical-induced fatty degen -eration and specific gene expression changes in rat liver.�@ �@ J. Toxicol. Sci�ɓ��e�� |
| 5�T��̗Y���b�g��p�����}�̑ΏƋy�щ�������28���Ԕ������^��̐t���i�玿�j�̈�`�q�����ʃf�[�^ | 204 | GSE87288 | Investigation of the early-response genes in chemical-induced renal carcinogenicity for the prediction of chemical carcinogenicity in rats. J. Toxicol. Sci�ɓ��e�� |
| 2-amino-4-nitrophenol��p�����Y���b�g��28���Ԕ������^�����ɂ�����t���i�����O�сj�̈�`�q�����ʂ̌o���I�ω� | 16 | GSE87394 | Time course analysis of outer medulla-specific gene expression profiles in the kidneys of Sprague-Dawley rats in a repeated dose study of 2-amino-4-nitrophenol. J. Toxicol. Sci�ɓ��e�� |
���f�[�^�����J���ꂽ�琏���lj����܂�
��Tox-Omics�ŊJ����������E�\�����s�����߂̃v���g�R�[��
�@Tox-omics project�̐��ʂƂ��āA�̓Ő��A�t�Ő��̔��ʋy�ѐt�����̗\�����ł���Tox-screen�V�X�e�����J�����܂��� (�_�E�����[�h��������)�B
�@�ڂ����菇�́A�������̃v���g�R�[�������Q�Ƃ��������B
�@�@�̓Ő��y�ѐt�Ő����ʖ@
�@�������� (28���Ԕ������^����) �œ���ꂽ�̑��y�ѐt���T���v������擾�����}�C�N���A���C�f�[�^�����ɍ\�z�������ʎ��ɓK�p���邱�ƂŁA�̑����тɐt���̈�ʓŐ������i���\�j�����o���A����Ƀ��[�_�[�`���[�g�`���Ŋ̑��y�ѐt���ɂ�����Y�������̒��x�����o�I�ɕ\�����邱�Ƃ��\�ƂȂ�܂��B�K�v�f�[�^����͂��邾���ŁA�}�Ɏ�������l���\������܂��B�l���傫���قǁA��`�q���x���ł͂��̓Ő��e��������Ă��邱�Ƃ������܂��i���ʒl�̍ŏ��l��0�j�B
| �� | �̑� | �t�� |
|---|---|---|
| 1 | �̍זE�P�זE�� | �玿�̔A�ǂ̋�E�ϐ� |
| 2 | �т܂̍זE��� | �玿�̔A�ǂ̊j�召�s�� |
| 3 | ���t���S���̍זE��� | �玿�̔A�ǂ̊j�Z�k |
| 4 | ���t���S���̍זE�ϐ� | �����O�т̔A�ǂ̒P�זE�� |
| 5 | ���t���Ӑ��̍זE���b�ϐ� | ������/�����ϐ� |
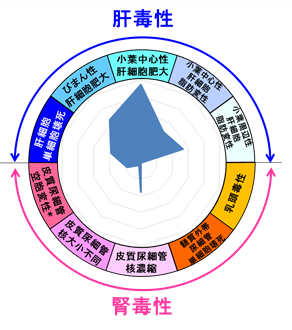
�k���ʐ��x�l
�@�{�v���W�F�N�g�ŗp����25�������̈�`�q�����ʃf�[�^���g���[�j���O�f�[�^�Ƃ��ėp�������̈�v����99.2% (96�`100%) �ł����B
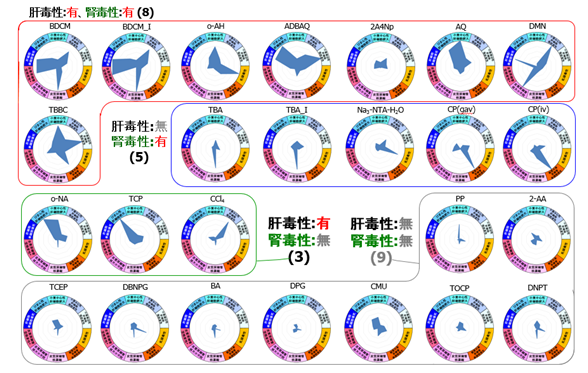
�@����ɁA�{�v���W�F�N�g�Ŏ擾����10�������̊O���f�[�^��p���ăo���f�[�V�����������ʁA��v����96.7% (80�`100%) �ƁA�Ő��Ǐ�ɉ��������ʂ������邱�Ƃ��m�F���Ă��܂��B
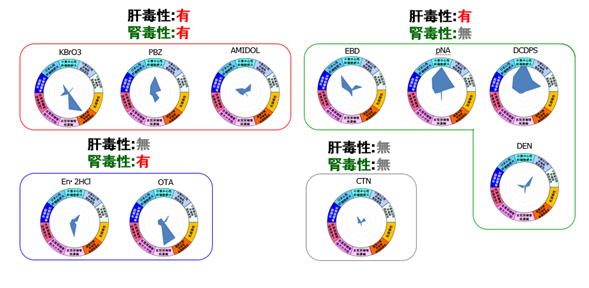
�A�t�����\���@
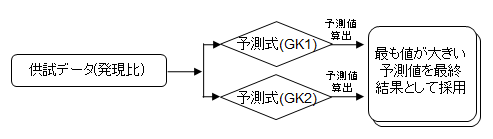
28���Ԕ������^�ɂ�蓾��ꂽ�t���T���v���̃}�C�N���A���C�f�[�^��{�v���W�F�N�g�ō\�z����2�̗\�����ɓK�p���邱�ƂŔ����\�����s���܂��B2�̗\���l���Z�o����܂����A�l���傫�������ŏI�I�ȗ\�����ʂƂȂ�܂� (���})�B
�K�v�f�[�^����͂��邾���ŁA�\���l���\������܂��B����ꂽ�\���l�����̒l�ł���ΐt������z���A���̒l�ł���ΉA���Ɣ��肳��܂��B
�k���ʐ��x�l

�g���[�j���O�f�[�^�y�ь��f�[�^��Concordance�͂��ꂼ��100%�A87.5%�ł���A�t������z�������ɂ��Ă͑S�Đ������\���ł��邱�Ƃ��m�F���Ă��܂��B
�B�̔����\���@
28���Ԕ������^�ɂ�蓾��ꂽ�̑��T���v���ɂ�����4��`�q�̔����ʕω�����PCR�@�ɂ�葪�肵�A4��̗\����`�q�̂����A�����ꂩ1��`�q�ł�2�{�ȏ�(3��`�q)��������1/2�{�ȉ�(1��`�q)�������A”�̔�������”�Ɣ��肵�܂���1�B�{��@�̓}�C�N���A���C�ɂ�鑪���K�v�Ƃ����A�ȈՂɎ��{���邱�Ƃ��ł��܂��B
��1�GSaito et al., J Toxicol Sci. 2016; 41, 383-90.
�k�̔����\���菇�l
�ڂ����菇�́A�������̃v���g�R�[�������Q�Ɖ������B
�@
�k���ʐ��x�l

�g���[�j���O�f�[�^�y�ь��f�[�^��Concordance�͂��ꂼ��82.8%�A86.4%�ł���A�g���[�j���O�f�[�^�Ɠ����x�̐��x�ŗ\���ł��邱�Ƃ��m�F���Ă��܂��B
���O�����\
���e�_��
Watanabe Y, Murakami T, Kawashima M, Hasegawa-Baba Y, Mizukami S, Imatanaka N, Akahori Y, Yoshida T, Shibutani M (2016) Maternal exposure to valproic acid primarily targets interneurons followed by late effects on neurogenesis in the hippocampal dentate gyrus in rat offspring. Neurotox. Res., (in press).
Abe H, Saito F, Tanaka T, Mizukami S, Watanabe Y, Imatanaka N, Akahori Y, Yoshida T, Shibutani M (2016) Global gene expression profiles in brain regions reflecting abnormal neuronal and glial functions targeting myelin sheaths after 28-day exposure to cuprizone in rats. Toxicol. Appl. Pharmacol., (in press).
Shiraki A, Tanaka T, Watanabe Y, Saito F, Akahori Y, Imatanak N, Yoshida T, Shibutani M (2016) Immunohistochemistry of aberrant neuronal development induced by 6-propyl-2-thiouracil in rats Toxicol. Appl. Pharmacol., (in press).
Shiraki A, Saito F, Akane H, Akahori Y, Imatanaka N, Itahashi M, Yoshida T, Shibutani M (2016) Gene expression profiling of the hippocampal dentate gyrus in an adult toxicity study captures a variety of neurodevelopmental dysfunctions in rat models of hypothyroidism. J. Appl. Toxicol., 36(1), 24–34.
Saito F, Matsumoto H, Akahori Y, Takeyoshi M (2016) Simpler alternative to CARCINOscreen® based on quantitative PCR (qPCR) J. Toxicol. Sci., 41(3), 383-390.
Matsumoto H, Saito F, Takeyoshi M (2015) Applicability of a gene expression based prediction method to SD and Wistar rats: An example of CARCINOscreen®. J. Toxicol. Sci., 40(6), 805-807.
Yamanaka H, Takeyoshi M (2015) Identification of sheep red blood cell (SRBC) surface immune-responsive peptides detected by antisera from SRBC immunized rat. J. Toxicol. Sci., 41(1), 13-16.
Yamashita K, Matsumoto H, Saito F, Takeyoshi M (2015) Differences in gene expression profiles in liver caused by different type of anesthesia; cases of CO2-O2 and isoflurane. J. Toxicol. Sci., 40(6), 829-836.
Abe H, Saito F, Tanaka T, Mizukami S, Hasegawa-Baba Y, Imatanaka N, Akahori Y, Yoshida T, Shibutani M (2015) Developmental cuprizone exposure impairs oligodendrocyte lineages differentially in cortical and white matter tissues and suppresses glutamatergic neurogenesis signals and synaptic plasticity in the hippocampal dentate gyrus of rats. Toxicol. Appl. Pharmacol., 290, 10-20.
Abe H, Tanaka T, Kimura M, Mizukami S, Imatanaka N, Akahori Y, Yoshida T, Shibutani M (2015) Developmental exposure to cuprizone reduces intermediate-stage progenitor cells and cholinergic signals in the hippocampal neurogenesis in rat offspring. Toxicol. Lett., 234(3), 180-193.
Akane H, Saito F, Shiraki A, Imatanaka N, Akahori Y, Itahashi M, Liyun W, Shibutani M (2014) Gene expression profile of brain regions reflecting aberrations in nervous system development targeting the process of neurite extension of rat offspring exposed developmentally to glycidol. J. Appl. Toxicol., 34(12), 1389-1399.
Matsumoto H, Saito F, Takeyoshi M (2014) CARCINOscreen®: New short-term prediction method for hepatocarcinogenicity of chemicals based on hepatic transcript profiling in rats. J. Toxicol. Sci., 39(5), 725-734.
Akane H, Saito F, Shiraki A, Takeyoshi M, Imatanaka N, Itahashi M, Murakami T, Shibutani M (2014) Downregulation of immediate-early genes linking to suppression of neuronal plasticity in rats after 28-day exposure to glycidol. Toxicol. Appl. Pharmacol., 279(2), 150-162.
Shiraki A, Saito F, Akane H, Takeyoshi M, Imatanaka N, Itahashi M, Yoshida T, Shibutani M (2014) Expression alterations of genes on both neuronal and glial development in rats after developmental exposure to 6-propyl-2-thiouracil. Toxicol. Lett., 228(3), 225-234.
Akane H, Shiraki A, Imatanaka N, Akahori Y, Itahashi M, Abe H, Shibutani M (2014) Glycidol induces axonopathy and aberrations of hippocampal neurogenesis affecting late-stage differentiation by exposure to rats in a framework of 28-day toxicity study. Toxicol. Lett., 224(3), 424-432.
Akane H, Saito F, Shiraki A, Imatanaka N, Akahori Y, Itahashi M, Wang L, Shibutani M (2014) Gene expression profile of brain regions reflecting aberrations in nervous system development targeting the process of neurite extension of rat offspring exposed developmentally to glycidol. J. Appl. Toxicol., 34(12), 1389-1399.
Akane H, Shiraki A, Imatanaka N, Akahori Y, Itahashi M, Ohishi T, Mitsumori K, Shibutani M (2013) Glycidol induces axonopathy by adult stage-exposure and aberration of hippocampal neurogenesis affecting late-stage differentiation by developmental exposure in rats. Toxicol. Sci., 134(1), 140–154.
Akane H, Saito F, Yamanaka H, Shiraki A, Imatanaka N, Akahori Y, Morita R, Mitsumori K, Shibutani M (2013) Methacarn as a whole brain fixative for gene and protein expression analyses of specific brain regions in rats. J. Toxicol. Sci., 38(3), 431-443.
Matsumoto H, Yakabe Y, Saito F, Saito K, Sumida K, Sekijima M, Nakayama K, Miyaura H, Otsuka M, Shirai T (2011) New short term prediction method for chemical carcinogenicity by hepatic transcript profiling following 28-day toxicity tests in rats. Cancer Informatics, 10, 259–271.
�w��\��
(����)
�V������.�@��`�q�����ʉ�͂ɂ�郁�J�j�Y���x�[�X�̊�/�t�Ő��]��. ���{�Ő��w��w�p�N��, 2016, ���É�.
���{���m.�@��`�q�����ʉ�͂ɂ�锭���\���ւ̒���. ���{�Ő��w��w�p�N��, 2016, ���É�.
Saito F. Japanese new project�Fassay developments by omics technologies. OECD Meeting of the Extended Advisory Group on Molecular Screening and Toxicogenomics (EAGMST), 2015, Paris, France.
Saito F. Tox-Omics project: Development of methods to detect multi-toxic effects using gene expression analysis. 9th World Congress on Alternatives and Animal Use in the Life Science, 2014, Prague, Czech.
Saito F. CARCINOscreen®: Novel short-term prediction system for carcinogenicity of chemicals by hepatic transcriptome analysis in a 28-day repeated dose toxicity study. 117th OMICS Group Conference. The International Conference on Genetic Engineering & Genetically Modified Organisms, 2013, Raleigh, NC, USA.
Kojima H. Japanese project “ARCH-Tox” for the future chemicals management policy: research and development of in vitro and in vivo assays for internationally leading hazard assessment and test methods. 15th Annual Congress of European Society for Alternatives to Animal Testing (EUSAAT), 2013, Linz, Austria.
Saito F. Tox-Omics Project: Development of mechanism based detection system for chemical-induced hepatotoxicity using gene expression analysis. OECD Meeting of the Extended Advisory Group on Molecular Screening and Toxicogenomics (EAGMST), 2012, Paris, France.
Saito F. Japanese new project�FAssay developments by omics technologies. AXLR8-3 workshop, 2012, Berlin, Germany.
���g����.�@�V�K�o�ώY�Əȃv���W�F�N�g�u��`�q�v���W�F�N�g�v ��24����{����������֖@�w��w�p���.�@�s�����J�u���u���{�ɂ������֖@�����̐V�����ٓ��v, 2011, �{��.
(�|�X�^�[)
�n糗m�S�A���コ�₩�A���J���{�q�A�Ԗx�L���A���c���L�ƁA�g�c�q���A�a�J�~. ���`���j�g���\�A�f28���Ԕ����o�����^�ɂ�郉�b�g�C�n�j���[�����V�������זE�n���̐_�o���זE����̍L�͂ȏ�Q���ɂ���. ���{�Ő��w��w�p�N�� (2016).
�ё��b�A���{���m�A�Ԗx�L���A�R������A�{�Y�p���A���яr�v�A�e�쒁�A�Έ䑏�q�A���䐽�A�V������. �Z�������X�N���[�j���O�@CARCINOscreen®��p������`�q�����ʃf�[�^�Ɋ�Â��i��ʓI�j ���X�N�]���@�̌���. ���{�Ő��w��w�p�N�� (2016).
Watanabe Y, Nakajima K, Hasegawa-Baba Y, Mizukami S, Akahori Y, Imatanaka N, Yoshida T, Shibutani M. Comparison in the effect on rat hippocampal neurogenesis between developmental exposure and postpubertal-stage exposure of N-methyl-N-nitrosourea. 14th European Congress of Toxicologic Pathology (ESTP) (2016).
������A�c���ҁA���؍ʎq�A�V������A�Ԗx�L���A���c���L�ƁA�g�c�q���A�a�J�~. ���b�g28���Ԕ������^�����̘g�g�݂ł̊C�n�j���[�����V���ɑ���E���U������Cuprizone�̏�Q���̌��o. ��31����{�Ő��a���w��w�p�W�� (2015).
������A�c���ҁA�V������A�Ԗx�L���A���g�����A���c���L�ƁA�g�c�q���A�a�J�~. ���⏝�Q�����N�v���]���̃��b�g�ւ̔��B���\�I�ɂ��]���ʂł̖ԗ��I��`�q������͂�p�����j���[�����E�O���A���B��Q�w�W�̌��o. ��42����{�Ő��w��w�p�N�� (2015).
�n糗m�S�A����q���A������A�c���ҁA���؍ʎq�A�ؑ��^�V�A���コ�₩�A����S���A�g�c�q���A�a�J�~. �o���v���_�̔��B���\�I�ɂ�郉�b�g�̊C�n�����̐���j���[�����V���ɗ^����e��. ��42����{�Ő��w��w�p�N�� (2015).
Hasegawa-Baba Y, Watanabe Y, Tanaka T, Shiraki A, Kimura M, Mizukami S, Abe H, Murakami T, Saito F, Akahori Y, Imatanaka N, Yoshida T, Shibutani M. Different toxicity targets in the hippocampal neurogenesis by developmental and postpubertal-stage exposure to valproic acid in rats. 13th European Congress of Toxicologic Pathology (ESTP) (2015).
Abe H, Tanaka T, Shirak A, Kimura M, Mizukami S, Saito F, Akahori Y, Imatanaka N, Yoshida T, Shibutani M. Evaluation of developmental neurotoxicity of cuprizone as a demyelinating agent in a framework of 28-day repeated oral toxicity study. 13th European Congress of Toxicologic Pathology (ESTP) (2015).
Shiraki A, Akane H, Itahashi M, Saito F, Akahori Y, Imatanaka N, Yoshida T, Shibutani M. Immunohistochemical detection of aberrant neuronal development induced by 6-propyl-2-thiouracil (PTU) in the framework of developmental neurotoxicity study and 28-day toxicity studies using rats. 13th European Congress of Toxicologic Pathology (ESTP) (2015).
Kojima H, Oshimura M, Imatanaka N. Update for Japanese project “ARCH-Tox” for the future chemicals management policy: Research and development of in vitro and in vivo assays for internationally leading hazard assessment and test methods. The American Society for Cellular and Computational Toxicology (ASCCT) (2015).
���؍ʎq�A�ԍ��O�q�A�V������A�Ԗx�L���A���c���L�ƁA���b�AWang Liyun�A����q���A��ؘa�F�A�g�c�q���A�a�J�~. 6-Propyl-2-thiouracil (PTU)�̃��b�g28���Ԕ������^�ɂ��b��B�@�\�ቺ������j���[�����E�O���A���B��Q�̌��o. ��30����{�Ő��a���w��w�p�W�� (2014).
������A���b�A�c���ҁA����q���A�V������A���g�����A���c���L�ƁA�g�c�q���A�a�J�~. �E���U�������N�v���]���̃��b�g�ւ̔��B���\�I�ɂ�闣�����̊C�n�j���[�����V���ɑ���e��. ��41����{�Ő��w��w�p�N�� (2014).
���؍ʎq�A�ԍ��O�q�A�V������A�Ԗx�L���A���c���L�ƁA���b�A����q���A�g�c�q���A�a�J�~ (2014, 9��9~12�����_��) 6-propyl-2-thiouracil (PTU)�̃��b�g���B���\�I�y��28���Ԕ������^�ɂ��b��B�@�\�ቺ������j���[�����E�O���A���B��Q�Ɋ֘A�����Q�w�W���q�̌���. ��157����{�b��w��w�p�W�� (2014).
Abe H, Itahashi M, Tanaka T, Kimura M, Mizukami S, Akahori Y, Imatanaka N, Yoshida T, Shibutani M. Impact of cuprizone as a demyelinating agent on rat hippocampal neurogenesis. ���ې_�o�a���w�� (2014).
�V������A���{���m�A���яr�v�A����R�܌��A���g�����A���c���L��. 2-Amino-4-ntrophenol��SD���b�g��28���Ԕ������^�����ɂ�����t�����ʕʂ̌o���I�Ȉ�`�q�����v���t�@�C�����. ��40����{�Ő��w��w�p�W�� (2013).
���{���m�A�V������A���g����. TGP�f�[�^��p�������w�����̒Z�������X�N���[�j���O�@:CARCINOscreen®�̌���. ��40����{�Ő��w��w�p�W�� (2013).
�ԍ��O�q�A�V������A���؍ʎq�A���b�AWang Liyun�A�Ԗx�L���A���c���L�ƁA��ؘa�F�A�O�X���q�A�a�J�~. �O���V�h�[���̃��b�g28���Ԕ������^�ɂ��C�n�j���[�����V���ւ̉e��. ��40����{�Ő��w��w�p�W�� (2013).
���؍ʎq�A�ԍ��O�q�A�V������A�Ԗx�L���A���c���L�ƁA���b�AWang Liyun�A��I�A��ؘa�F�A�O�X���q�A�a�J�~. 6-propyl-2-thiouracil (PTU) �̃��b�g���B���\�I�ɂ��b��B�@�\�ቺ������j���[�����E�O���A���B��Q�Ɋ֘A�����`�q�����v���t�@�C���̈قȂ�]���ʂł̓��� ��29����{�Ő��a���w��w�p�W�� (2013).
�ԍ��O�q�A�V������A���؍ʎq�A���b�AWang Liyun�A��ؘa�F�A�O�X���q�A�a�J�~. �O���V�h�[���̃��b�g�ւ�28���Ԕ������^�ɂ��C�n�����ɂ�����j���[�����V���ɑ���e��. ��29����{�Ő��a���w��w�p�W�� (2013).
�ԍ��O�q�A�V������A�R���G���A���؍ʎq�A��I�AWang Liyun�A�ѐm���A��ؘa�F�A�O�X���q�A�a�J�~. ���b�g�̔]���ʓ��ٓI�Ȗԗ��I��͂��\�Ƃ��郁�^�J�[���S�]�Œ�@�̌���. ��28����{�Ő��a���w��w�p�W�� (2012).�@
���؍ʎq�A�ԍ��O�q�A�V������A�R���G���ALiyun Wang�A��I�A��ؘa�F�A�O�X���q�A�a�J�~. 6-propyl-2-thiouracil (PTU)�̔��B���\�I�ɂ�郉�b�g�C�n�����ɂ�����b��B�@�\�ቺ������j���[�����V���̉i���I�ȉe�����o�Ƃ��̈�`�q�����v���t�@�C���̓���. ��39����{�Ő��w��w�p�W�� (2012).
�ԍ��O�q�A�V������A�R���G���A���؍ʎq�A���c��q�A���M�G�T�A�J���}���q�A��ؘa�F�A�O�X���q�A�a�J�~. �O���V�h�[���̃��b�g�ꓮ���\�I�ɂ��ꓮ���Ǝ������̐_�o�n�ɑ���e��. ��39����{�Ő��w��w�p�W�� (2012).
Kojima H, Tanaka N, Oshimura M, Saito K, Saito F and Imatanaka N. New research projects in Japan for alternative to repeated dose oral toxicity studies. EUROTOX 2012- 48th Congress of the European Societies of Toxicology (2012).
Kojima H, Tanaka N, Oshimura M, Saito K, Saito F, Imatanaka N. Japanese new project “ARCH-Tox” for the future chemicals management policy: Research and development of in vitro and in vivo assays for internationally leading hazard assessment and test methods. 1st annual Meeting of the American Society for Cellular & Computational Toxicology (2012).
�V������A���{���m�A���g����. CARCINOscreen®: New short-term prediction method for carcinogenicity by hepatic transcript profiling in a 28-day repeat-dose toxicity study. ���������w�A�����. ���{�o�C�I�C���t�H�}�e�B�N�X�w��N�� (2012).
���{���m�A�V������A���g����. ���w�����̒Z�������X�N���[�j���O�̗p�ʐݒ���@�̌���. ��39����{�Ő��w��w�p�N�� (2012).
�V������A���{���m�A���g�����A����F�B. �Z�������\���V�X�e����Wistar Hannover���b�g�ւ̓K�p���y�ьn���ԍ��̌���. ��39����{�Ő��w��w�p�N�� (2012).
Akane H, Saito F, Shiraki A, Mitsumori K, Shibutani M. Effect of maternal exposure to glycidol on nervous system of dams and offspring in rats. 30th Meeting of the European Society of Veterinary Pathology, Annual Meeting of the European College of Veterinary Pathologist 24th Annual Meeting of the Spanish Society of Veterinary Pathology (2012).
���؍ʎq�AWang Liyun�A��I�A�ԍ��O�q�A�y���얁�A�k��F���A��ؘa�F�A�O�X���q�A�a�J�~. ���B���Ȃ������n��ł̍b��B�@�\�ቺ�ɂ�郉�b�g�C�n�����ɂ�����j���[�����V���ւ̉e���̔�r. ��152����{�b��w��w�p�W�� (2011).
![CERI ��ʍ��c�@�l ���w�����]�������@�\](../img/ceri_logo.png)