業務案内
PIC/S GMP対応支援 洗浄バリデーションのための医薬品原薬のPDE設定
PIC/S GMP対応支援 洗浄バリデーションのための医薬品原薬のPDE設定
医薬品をマルチパーパスプラント(多目的設備、共用施設)において製造する際、洗浄評価基準の設定が重要となります。EU-GMP及びPIC/Sでは、洗浄評価において毒性学的評価に基づく「健康ベースばく露限度値(Health-Based Exposure Limits(HBELs)」の設定が求められており、医薬品製造において、固有の毒性情報に基づくPDE設定、洗浄評価基準の設定の重要性が高まっています。また、労働安全衛生の観点からも、毒性情報に基づく適切な許容ばく露濃度(OEL)の設定が重要となります。
PDEとは?
Permitted Daily Exposure
ばく露がたとえ一生涯続いたとしても、それ以下の用量では健康に対する悪影響が予想されない物質固有の一日ばく露量
-
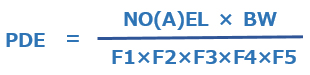
- NOAEL: No-observed adverse effect level (mg/kg/day)
BW: 体重 (通常50kg)
調整係数
F1: 種間の外挿を考慮した係数
F2: 個人間のばらつきを考慮した係数
F3: 毒性試験の期間を考慮した変数
F4: 影響の重篤性を考慮した係数
F5: NO(A)ELが得られない場合に適用する変数
CERIでは、最新の評価ガイドライン1)に従った原薬のPDE設定が可能です。また、PDE設定の評価プロセスをPDE設定検討会2)により検討・推奨された様式に沿った「PDE設定報告」の形式で報告書を作成します。
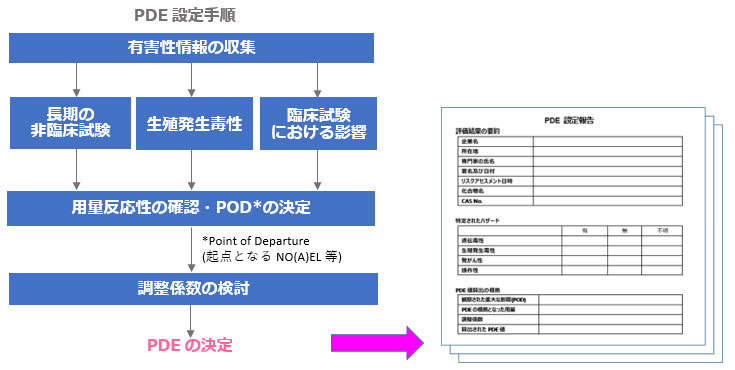
1) 評価ガイドライン
ICH: Guideline for residual solvents (Q3C)/ Guideline for elemental impurities (Q3D)
EMA: Guideline on setting health based exposure limits for use in risk identification in the manufacture of different medicinal products in shared facilities
ISPE: Risk-Based manufacture of pharmaceutical products
PIC/S: Guidelines on setting health based exposure limits for use in risk identification in the manufacture of different medicinal products in shared facilities (PI 046-1)
ASTM E3219-20: Standard Guide for derivation of Health-Based Exposure Limits (HBELs)
2) PDE設定検討会
科学的根拠に基づく医薬品の交叉汚染限度値としてGMPで要求されているPDE設定の考え方について業界で一定の共通認識を醸成することを目的とした製薬関連企業のPDE設定関係者などのメンバーで構成される検討会
