業務案内
CERIのプロテオーム解析
応用
- 定量プロテオーム解析
- Exosomeの解析
- FFPE組織サンプルの解析
- バイオマーカー探索
- バイオ医薬品中の不純物解析
- バイオ医薬品の糖鎖分析
- フォーカスドプロテオミクス
- 膜タンパク質の解析
- P-450の多型解析
- タンパク質複合体の解析
- 糖鎖分析
- 二次元電気泳動データベース
- アダクトの解析
定量プロテオーム解析
CERIの定量プロテオ−ム解析は、目的に応じて網羅的な定量比較解析(iTRAQ、SILAC等の安定同位体ラベル又はノンラベル定量)、ターゲットタンパク質の相対定量(MRM解析)又はターゲットタンパク質の絶対定量(AQUAペプチド等の安定同位体ラベルペプチドを使用したMRM解析)の中から適切な方法を選択することが可能です。
特にLFQ解析においては、5年間に渡って蓄積したDDA法(データ依存性解析)で取得した500万を超えるスペクトル及びクロマトグラムのデータベースを用いて、DIA法で参照するための内部データベースを構築しております。このDIA用内部データベースを参照することで、信頼性の高いDIA(データ非依存性解析)法による定量比較解析を実施することが可能です。
Exosome(エクソソーム)の解析
各種培養細胞の上清中、実験動物やヒトの尿、血清、唾液、涙液をはじめ植物等にも存在するExosome(エクソソーム)のnanoUPLC-ESI-MS/MSを用いたショットガン解析や2D-DIGE: 2-D Fluorescence Difference Gel Electrophoresis (蛍光標識二次元ディファレンスゲル電気泳動解析)を用いた比較解析を実施いたします。エクソソームの抽出、精製から受託することも可能です。
オプションとして、エクソソーム量及び精製度の確認をMalvern Panalytical社製NanoSight NS300を使用したトラッキング解析*で粒度分布、粒子径、粒子数濃度を求めることにより実施いたします。また、CD9等のエクソソームマーカーを用いたELISAでの確認も可能です。
*NanoSight NS300を用いたトラッキング解析は、日本カンタム・デザイン株式会社で実施いたします。

FFPE組織サンプルの解析
ホルマリン固定パラフィン包埋(FFPE: Formalin-Fixed Paraffin-Embedded)組織からタンパク質を抽出して、2D-DIGE: 2-D Fluorescence Difference Gel Electrophoresis (蛍光標識二次元ディファレンスゲル電気泳動解析)、SDS-PAGE又は、nanoUPLC-ESI-MS/MSによるショットガン解析で比較解析を行います。
オプションとしてLMD*(レーザーマイクロダイセクション:Leica Microsystems社製 LMD7000を使用)で取得した微小部位間の比較解析を実施可能です。LMDで取得した数μm2の細胞内小器官(オルガネラ)等の微小部位から数百タンパク質の発現比較が可能です。
*LMD7000を使用したサンプルの採取は、株式会社テクノプロ テクノプロ・R&D社で実施いたします。

https://researchcenter-technopro.com/
バイオマーカー探索
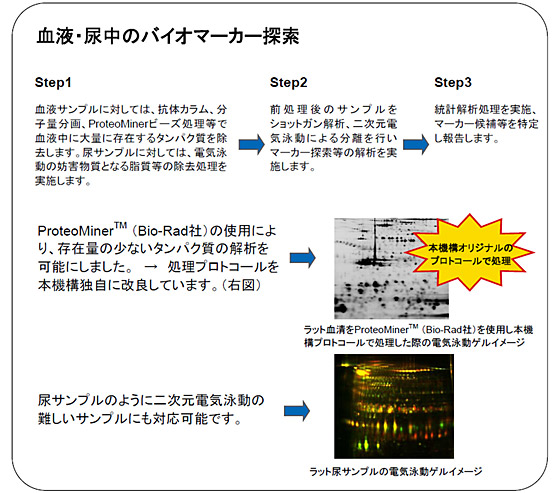
ヒト臨床サンプルや疾患モデル動物を用いて、血液、尿、髄液などにおけるタンパク質を解析することにより、病態と連動して変動するタンパク質を同定し、疾患バイオマーカーの発見につなげる疾患プロテオミクス研究が注目されています。疾患プロテオミクスの対象とする測定サンプルとしては、採取の容易さなどから特に血液サンプルでの研究が最も盛んに行なわれています。血液中のタンパク質は、22種類の主要タンパク質で99%が構成されており疾患マーカーとして重要なタンパク質の多くは残り1%のなかに含まれているため、疾患マーカーの探索が困難となっています。
本機構では、抗体カラム、分子量分画、ProteoMinerビーズ処理等の方法を用いた主要タンパク質を除去して微量の疾患マーカーを効果的に探索する独自の技術を開発しています。本手法は、尿試料及び培養上清中の血清の処理にも適用可能です。 (培養上清の分子量分画を実施した例)
-
- 血液・尿中のバイオマーカー探索
- 学会発表 2010年 日本ヒトプロテオーム機構第8回大会
松寿仙長期投与により増減するラット血清中タンパク質の解析
抗体カラム処理後の血中タンパク質の2D-DIGEを用いた定量比較の再現性評価
バイオ医薬品中の不純物解析
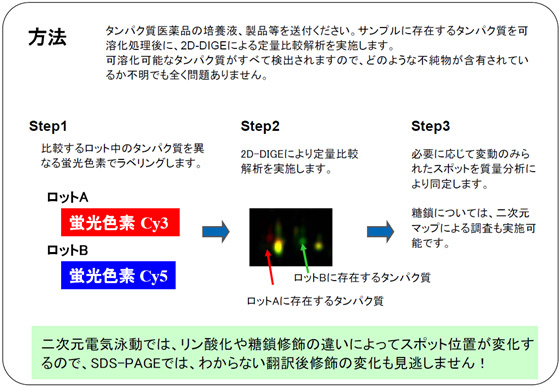
本機構では、タンパク質医薬品の製造工程に由来するタンパク質性不純物や目的タンパク質の分子変化体の高感度検出、高精度な定量比較に最適な2D-DIGEを利用した「タンパク質医薬品中の不純物解析」を実施しています。
製造工程の各段階における不純物の解析、製造工程の変更に伴う不純物のロット間差の管理に有用な方法です。
-
- 不純物解析方法
バイオ医薬品の糖鎖分析
IgGやエリスロポエチンなどといった糖タンパク質性のバイオ医薬品の承認申請には、タンパク質と結合している糖鎖のプロファイリングや糖組成の分析が必要になります。本機構では糖組成分析や多次元HPLC分析によるバイオ医薬品の糖鎖プロファイリングを受託試験として実施しています。
フォーカスドプロテオミクス
さまざまな前処理と2D-DIGE及びLC-MS/MSを組み合わせて、以下のタンパク質にプロテオーム解析を受託しています。
| 目的タンパク質 | 前処理法 |
|---|---|
|
・ リン酸化タンパク質(ペプチド) ・ 糖タンパク質(ペプチド) ・ ユビキチン化タンパク質 ・ 酸化タンパク質 ・ ミトコンドリア、核等のオルガネラ ・ P450等の膜タンパク質 |
IMAC(イオンメタルアフィニティークロマトグラフィー) レクチンアフィニティークロマトグラフィー 抗ユビキチン化抗体カラム カルボニルタンパク質濃縮カラム ショ糖濃度勾配による遠心分離 溶解性による分画 |
- 学会発表 2009年日本ヒトプロテオーム機構第7回大会
Chip-Based Infusion法によるユビキチン化タンパク質の多型解析 - 論文発表
Yamanaka, H., Takeyoshi, M., Minobe, Y., Yakabe, Y., Takatsuki, M., Sato, H., Drug Metabolism Letters, 1, 281-286 (2007)
Yamanaka, H., Yakabe, Y., Saito, K., Sekijima, M.,Shirai, T., Quantitative proteomic analysis of rat liver for carcinogenicity prediction in a 28-day repeated dose study. Proteomics 7, 781-795 (2007).
Yamanaka, H., Minobe, Y., Yakabe, Y., Saito, K., Sekijima, M., Shirai, T., High-accuracy Prediction of Carcinogenicity by Global Quantitative Analysis of Post-translational Modifications in a 28-Day In Vivo Rat Study. Cancer Genomics & Proteomics 5, 105-116 (2008)
膜タンパク質の解析
P450等の膜タンパク質を二次元電気泳動で解析することは、種々の界面活性剤が開発された現在でも困難な課題の一つです。本機構では、上記のフォーカスプロテオミクスでは膜タンパク質のみを溶解性により分画後にショットガン解析を実施する選択的ショットガン法または2D-DIGEによる同定法を開発しています。この手法を用いて、33種のP450タンパク質を同定し、定量分析が可能となっています。
二次元電気泳動での測定が難しく、バイオマーカーが発見できなかった場合等、是非お試しください。
-
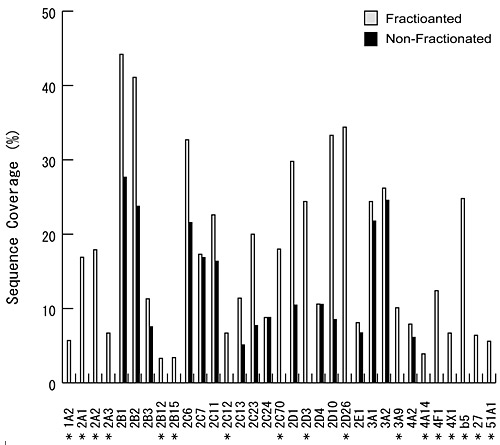
- 図 CYPアイソフォームの検出例
黒:分画後のMS解析検索結果、灰色:分画前のMS解析検索結果
* 分画前に検出されず、分画後に検出されたアイソフォーム
P-450の多型解析
CYPアイソフォームの解析は、新薬の臨床試験における薬物相互作用の検討、個々の患者に対するオーダーメード医療における診断等の目的に必須であり、CYPアイソフォームの質量分析装置を用いたプロテオーム解析研究が注目されています。CYPアイソフォームの網羅的解析では、CYPスーパーファミリーの1次構造が非常に近似していることが解析を困難にする要因の1つとして考えられますが、本機構ではこれまでの研究から、構造近似性に由来する物理化学的な性状の近似性を解析に利用し、ヒト及びラット肝ミクロソームを溶解性に基づいて分画した後に、各画分に含まれるタンパク質をMS/MSにより一斉同定することによって膜タンパク質であるCYPを難溶解性画分に濃縮、発現しているCYPアイソフォームの網羅的かつ定量的な解析を受託試験として実施しています。
CYPアイソフォームの同定に加えて、質量分析データのデータベース検索アルゴリズムを改良してアミノ酸配列のシークエンシングによって、タンパク質レベルで一塩基多型解析(SNPs: Single Nucleotide Polymorphisms)に対応する一アミノ酸置換(SAPs:single amino acid polymorphisms)の質量分析データから直接的に解析可能としています。
タンパク質複合体の解析
タンパク質の機能解析には、相互作用するパートナーを同定することが欠かせません。免疫沈降法や様々なタンデムアフィニティ精製(TAP)法により精製したタンパク質複合体混合物にショットガン法を用いることによってタンパク質複合体を形成しているパートナータンパク質を網羅的に同定します。また、得られたタンパク質複合体中の特定のタンパク質の翻訳後修飾を二次元電気泳動によって解析することも可能です。
糖鎖分析
近年では従来のプロテオーム解析だけでなく、糖鎖をはじめとした翻訳後修飾の解析が注目されています。なかでも多くのタンパク質には糖鎖が付与されており、糖鎖はタンパク質の体内動態の決定や安定性の向上・生理活性の調節など重要な役割を果たしていることから、特に注目を集めています。特に、エリスロポエチンなどといった糖タンパク質性のバイオ医薬品の承認申請には、タンパク質と結合している糖鎖のプロファイリングや糖組成の分析が必要になります。
本機構では、タンパク質の翻訳後修飾の解析の一つとして、糖組成分析や多次元HPLC分析による糖鎖の分析を受託試験として実施しています。
- 糖組成分析
- 多次元HPLC分析
二次元電気泳動データベース
本機構では、種々の動物種の肝臓、血液についての二次元電気泳動データベースを作成することによって、どのスポットがどのタンパク質に該当するのかが分かっていれば二次元電気泳動(2D-DIGE)をマイクロアレイのように使用可能であることから、種々の動物種の肝臓、血液をはじめとする様々なサンプルの二次元電気泳動データベースを構築し、活用しています。本機構では、5000スポット以上の二次元電気泳動法で分離されたタンパク質を同定しています(データの一部は、NEDOトキシコゲノミクスプロジェクトの中で取得したものです)。
以下のPDFに、本機構の二次元電気泳動データベースに登録しているタンパク質の一部についてタンパク質名の一覧表を示しました。
二次元電気泳動データベース
タンパク質アダクトの解析
特異体質性薬物毒性(IDT:Idiosyncratic drug toxicity)と総称される副作用発現の最初のステップとして生体内で生成した薬物の反応性代謝物とタンパク質との共有結合体(アダクト)の存在が明らかにされています。本機構では、RI標識化合物の反応性代謝物とタンパク質が形成するアダクトを二次元電気泳動法により分離してRIイメージを取得し、アダクトを形成したタンパク質を高精度に同定する独自の手法を開発しています。
- 学会発表 2009年 日本薬物動態学会 第24回年会
Proteomic analysis of the insoluble protein adducts induced by reactive metabolites
